Στην έγκριση κυκλοφορίας του mCombriax στην ΕΕ, του πρώτου συνδυασμένου εμβολίου εποχικής γρίπης και COVID-19 που βασίζεται στην τεχνολογία mRNA και το οποίο προστατεύει άτομα ηλικίας 50 ετών και άνω προχώρησε ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ). Το εμβόλιο κατασκευάζει η Moderna Biotech, με έδρα την Ισπανία.
Σύμφωνα με τη ανακοίνωση του ΕΜΑ, η έγκριση του συνδυαστικού mRNA εμβολίου είναι σημαντική, καθώς, τόσο ο COVID-19, όσο και η γρίπη είναι μεταδοτικές ασθένειες που επηρεάζουν κυρίως το αναπνευστικό σύστημα, προκαλώντας συμπτώματα όπως βήχας, συμφόρηση της μύτης, πυρετό και ρίγη. Αν και οι περισσότερες περιπτώσεις είναι ήπιες ή μέτριες, σοβαρές επιπλοκές μπορεί να εμφανιστούν, ειδικά σε ηλικιωμένους και άτομα με εξασθενημένο ανοσοποιητικό σύστημα. Η συνλοίμωξη από τον ιό της γρίπης και τον SARS-CoV-2 (που προκαλεί τον COVID-19) μπορεί να οδηγήσει σε πιο σοβαρή νόσηση από ό,τι η μόλυνση από τον καθένα ξεχωριστά.
Σύμφωνα με τα τελευταία επιστημονικά δεδομένα του Παγκόσμιου Οργανισμού Υγείας (ΠΟΥ), μέχρι την 1η Φεβρουαρίου 2026, στην Ευρώπη είχαν καταγραφεί 281.728.062 κρούσματα COVID-19, ενώ η εποχική γρίπη αποτελεί επίσης σημαντικό φορτίο, με έως και 50 εκατομμύρια συμπτωματικά κρούσματα ετησίως στην Ευρωπαϊκή Οικονομική Ζώνη (ΕΟΧ).
Σύμφωνα με τον ΕΜΑ, το mCombriax λειτουργεί όπως και άλλα εμβόλια, προετοιμάζοντας τον οργανισμό να αμυνθεί εναντίον των ιών, καθώς περιέχει mRNA με οδηγίες για την παραγωγή πρωτεϊνών που βρίσκονται στον SARS-CoV-2, καθώς και τους ιούς της γρίπης τύπου A-H1N1, τύπου A-H3N2, καθώς και της γρίπης τύπου B (Victoria lineage). Ως το πρώτο συνδυασμένο εμβόλιο κατά του COVID-19 και της γρίπης, το mCombriax προσφέρει την δυνατότητα μιας μόνο ένεσης για προστασία από και τις δύο ασθένειες.
Η σύσταση του EMA βασίζεται σε δεδομένα που δείχνουν ότι το mCombriax προκαλεί την παραγωγή επαρκών αντισωμάτων τόσο εναντίον του SARS-CoV-2 όσο και των ιών της γρίπης. Σε μια κύρια μελέτη με 8.000 συμμετέχοντες ηλικίας 50 ετών και άνω, τα επίπεδα αντισωμάτων ήταν στατιστικά ισοδύναμα με αυτά που παρατηρήθηκαν σε άτομα που έλαβαν ξεχωριστά τα εμβόλια Spikevax (για τον COVID-19) και Fluzone HD/Fluarix (για τη γρίπη).
Οι πιο συχνές παρενέργειες (που μπορεί να επηρεάσουν περισσότερο από 1 στα 10 άτομα) περιλαμβάνουν πόνο στο σημείο της ένεσης, κόπωση, μυϊκούς πόνους, πονοκέφαλο, ρίγη, πρησμένους λεμφαδένες, ναυτία, έμετο και πυρετό. Οι ανεπιθύμητες ενέργειες εμφανίζονται συνήθως εντός 2 ημερών και διαρκούν κατά μέσο όρο 3 ημέρες.
Όσον αφορά τη σημερινή εξέλιξη, η θετική γνώμη του EMA αποτελεί ενδιάμεσο στάδιο για την έγκριση του mCombriax. Η απόφαση θα σταλεί στην Ευρωπαϊκή Επιτροπή για την τελική έγκριση κυκλοφορίας σε όλη την ΕΕ, ενώ μετά την έγκριση, κάθε κράτος-μέλος θα αποφασίσει για την τιμολόγηση και την αποζημίωση του εμβολίου, λαμβάνοντας υπόψη τις εθνικές ανάγκες υγείας, καθιστώντας το mCombriax μια επιπλέον επιλογή για τις εθνικές αρχές υγείας, οι οποίες θα αποφασίσουν για την ενσωμάτωσή του στα εμβολιαστικά προγράμματα, ανάλογα με την επιδημιολογική εικόνα κάθε κράτους μέλους.
Πηγή: ΚΥΠΕ
EMA Approves First Combined COVID-19 and Flu Vaccine
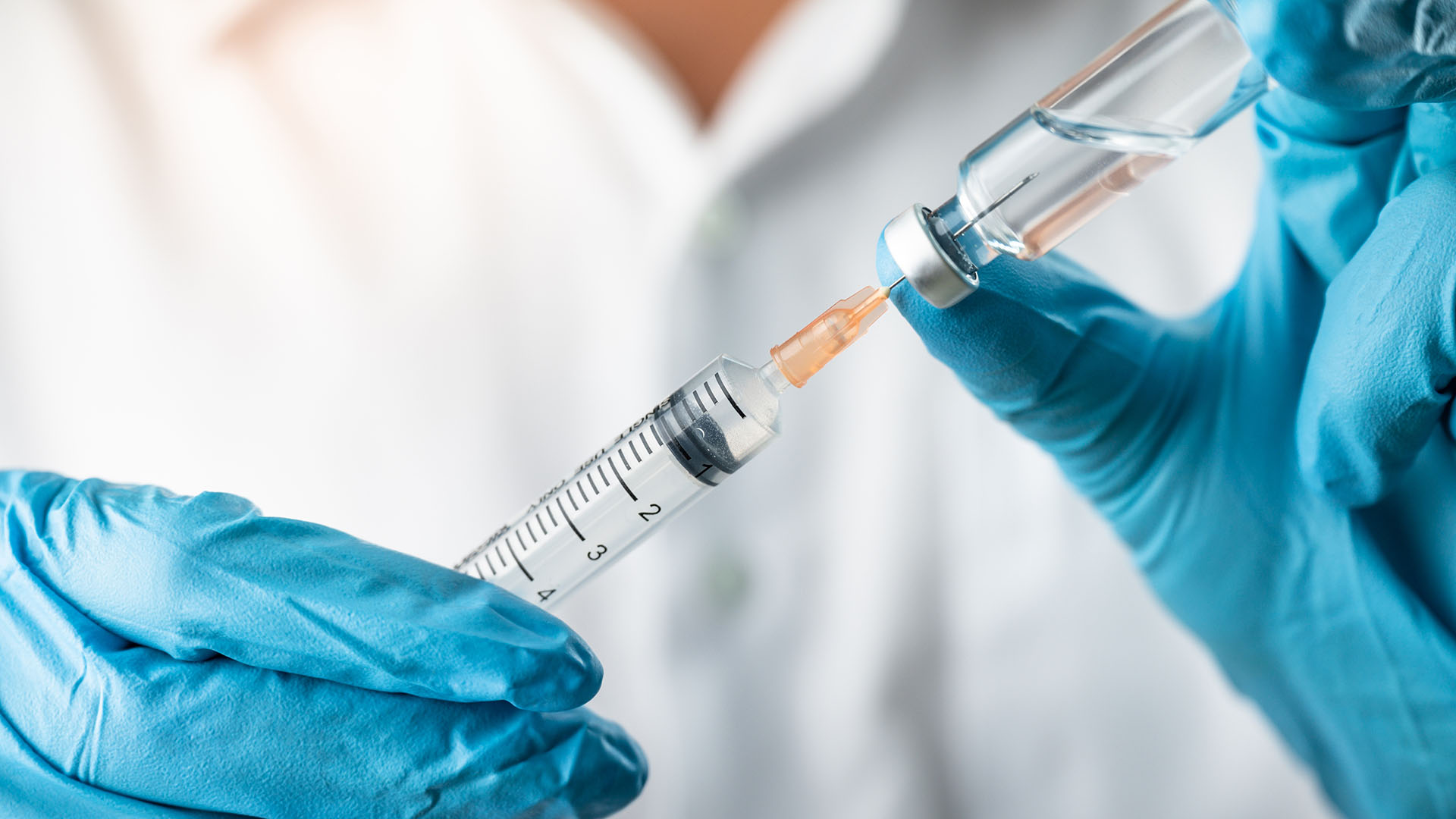
The European Medicines Agency (EMA) has approved mCombriax, the first combined vaccine for COVID-19 and influenza based on mRNA technology. The vaccine is intended for people aged 50 and over and was developed by Moderna Biotech. The approval is considered significant as both COVID-19 and influenza are contagious respiratory diseases, with potential serious complications, especially in the elderly and people with weakened immune systems. mCombriax works by preparing the body to defend against viruses, containing mRNA with instructions for producing proteins found in SARS-CoV-2 and influenza viruses of type A-H1N1, A-H3N2, and type B. Clinical trials showed that the vaccine induces adequate antibody production against both viruses, with levels comparable to those observed in people who received separate vaccines for COVID-19 and influenza. The most common side effects include pain at the injection site, fatigue, muscle aches, headache, chills, swollen lymph nodes, nausea, vomiting, and fever, which usually last a few days. The EMA approval is an intermediate step, and the final marketing authorization throughout the EU will be given by the European Commission. After approval, each member state will decide on the pricing and reimbursement of the vaccine, taking into account national health needs. mCombriax offers a single solution for protection against COVID-19 and influenza, and is expected to be an additional option for vaccination programs.
Similar Articles

ΕΜΑ: Εγκρίνει το πρώτο συνδυασμένο εμβόλιο κατά COVID-19 και εποχικής γρίπης
Feb 27
You Might Also Like

Έγκριση δεύτερης δέσμης SAFE για την Ελλάδα από το ECOFIN
Feb 17

«Μου φέρθηκαν σαν σκυλί, δεν είμαι μαριονέτα κανενός»
Feb 17

Γεφύρωση του χάσματος: Κατανόηση και δράση κατά του κινδύνου εμφάνισης έρπητα ζωστήρα
Feb 19
Νέα μελέτη εξηγεί πώς προκαλείται η σπάνια θρόμβωση μετά από εμβόλια Covid-19
Feb 25

ΕΜΑ: Εγκρίνει το πρώτο συνδυασμένο εμβόλιο κατά COVID-19 και εποχικής γρίπης
Feb 27